Por Marta López García* (CSIC)
Afirmar que los parásitos son fascinantes no solo es atrevido, sino que es poco frecuente. Solemos verlos como seres dañinos y nos produce rechazo escuchar la palabra. Sin embargo, desde un punto de vista científico, los parásitos son seres increíbles porque tienen una gran diversidad de formas de vida y sus adaptaciones les permiten vivir dentro de otros organismos (hospedadores). Y esta asombrosa capacidad de moverse entre los hospedadores para asegurar su supervivencia es lo que les hace fascinantes en términos biológicos.

Desde el Instituto de Recursos Naturales y Agrobiología de Salamanca (IRNASA-CSIC) se trabaja para frenar esta enfermedad
Sin embargo, los parásitos también pueden tener consecuencias muy negativas para la salud y el bienestar del ser humano y los animales. Por eso, conocer su compleja biología supone un gran reto científico en la actualidad. Ante su elevada prevalencia global es necesario desarrollar herramientas de prevención y control frente a ellos.
En este sentido, desde el Instituto de Recursos Naturales y Agrobiología de Salamanca (IRNASA-CSIC), trabajamos para frenar la fasciolosis. Esta enfermedad, causada por gusanos del género Fasciola, especialmente Fasciola hepatica, afecta principalmente al ganado ovino y bovino. Tiene una alta prevalencia en Castilla y León, al estar presente hasta en el 50% del ganado. Además, puede infectar a los seres humanos y, de hecho, es considerada una enfermedad emergente porque se encuentra en más de 2,5 millones de personas y 17 millones están en riesgo de infección.
La relación entre ‘Fasciola hepatica’ y hospedador
Fasciola hepatica es el protagonista de nuestra investigación. Se trata de un gusano plano, con forma de punta de lanza, que puede medir hasta 5 cm de largo y 1,5 de ancho cuando es adulto. Trabajamos para conocer las bases moleculares que rigen la infección del parásito dentro del hospedador vertebrado.

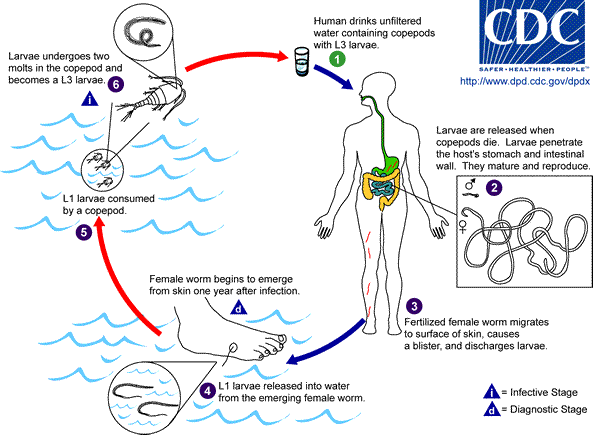
Tras ingerir el hospedador alimentos o agua contaminados con las formas infectivas de Fasciola hepatica (formas larvales denominadas metacercarias) se inicia la infección. Cuando estas alcanzan el intestino, salen del quiste como gusanos juveniles y son capaces de atravesar la pared del intestino delgado hasta la cavidad peritoneal, donde inician una compleja ruta de migración hasta el hígado. Allí se mantienen durante mucho tiempo creciendo al alimentarse del tejido hepático. Finalmente llegan a la vesícula biliar, donde se convierten en parásitos adultos y liberan huevos al medio ambiente, a través de las heces del animal, para completar su ciclo de vida.
La patología asociada a la enfermedad se relaciona con la presencia de los parásitos en el hígado. A medida que se alimentan del parénquima hepático (el componente del hígado que filtra la sangre para eliminar las toxinas) pueden causar inflamación y daño en el hígado con síntomas como dolor abdominal, diarrea, fiebre, pérdida de peso y, en los casos más graves, hepatitis, fibrosis y cirrosis. Aunque las infecciones en humanos suelen ser menos comunes que en el ganado, pueden ser graves si no se tratan adecuadamente. En cuanto a las perspectivas de tratamiento, existen medicamentos antiparasitarios, como el triclabendazol para tratarla tanto en seres humanos como en ganado. Sin embargo, cada vez se muestran más indicios de resistencia del parásito, por lo que disminuye la eficacia de este fármaco. Por la complejidad del ciclo biológico del parásito y su inminente resistencia a los fármacos necesitamos nuevas herramientas de control como las vacunas. Desde el laboratorio, tratamos de replicar el ciclo de vida de Fasciola hepatica para desentrañar las moléculas clave que utiliza durante su infección. Esto nos permite conocer qué molécula podría ser una buena candidata para desarrollar una vacuna en los animales frente a la fasciolosis.

Fasciola hepatica afecta principalmente al ganado ovino y bovino / Máximo López Sanz
Sin embargo, como en muchas enfermedades infecciosas, la prevención sigue siendo la clave y es necesario promover prácticas adecuadas de higiene (evitar la ingestión de alimentos y agua contaminada) para reducir la exposición a los parásitos y combatir así la enfermedad.
Como hemos visto, los parásitos son organismos fascinantes que han coexistido con el ser humano desde tiempos inmemoriales, en este caso a través de uno de sus principales sustentos: el ganado. Los estudios sobre los parásitos nos ofrecen una valiosa información sobre la biología y la evolución de sus hospedadores. Por ello, aunque los parásitos no son organismos bienvenidos, sin lugar a duda, nos brindan un gran conocimiento sobre las complejidades de la vida en nuestro planeta.
*Marta López García es investigadora del Instituto de Recursos Naturales y Agrobiología de Salamanca (IRNASA-CSIC).